Массовое число атома меди, в ядре которого содержится 36 нейтронов, равно:
Массовое число атома кальция, в ядре которого содержится 22 нейтрона, равно:
Атому металла в основном состоянии соответствует электронная конфигурация:
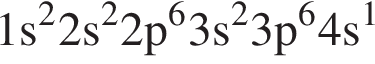
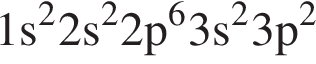
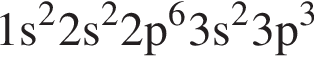
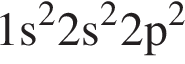
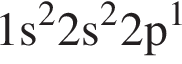
Атому металла в основном состоянии соответствует электронная конфигурация:
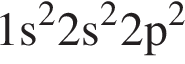
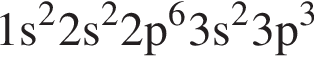
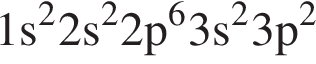
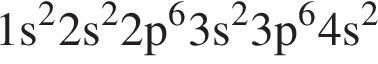
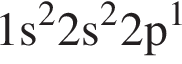
В периодической системе в одном периоде с бромом находится элемент:
Электронная конфигурация атома в основном состоянии 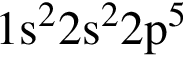 . Число протонов в атоме равно:
. Число протонов в атоме равно:
Анион серы ![]() содержит столько же электронов, сколько и атом:
содержит столько же электронов, сколько и атом:
Одноатомными молекулами (н. у.) образовано простое вещество:
Заряд ядра химического элемента +35. Его относительная атомная масса равна:
Установите соответствие между электронной конфигурацией внешнего энергетического уровня атома (иона) в основном состоянии и названием частицы.
1 — 3s23p6
2 — 3s23p2
3 — 2s22p6
а — катион натрия
б — атом кремния
в — хлорид-ион
г — атом кислорода
д — атом гелия
Наименьшее число протонов содержится в ядре атома, название которого:
Формула высшего оксида элемента А-группы ![]() Укажите формулу электронной конфигурации внешнего энергетического уровня атома элемента
Укажите формулу электронной конфигурации внешнего энергетического уровня атома элемента ![]() в основном состоянии:
в основном состоянии:
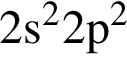
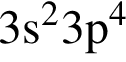
Согласно положению в периодической системе наиболее выраженные металлические свойства проявляет элемент, электронная конфигурация внешнего энергетического уровня которого в основном состоянии:
Одноатомными молекулами (н. у.) образовано простое вещество:
Заряд ядра химического элемента +28. Его относительная атомная масса равна:
Установите соответствие между электронной конфигурацией внешнего энергетического уровня атома (иона) в основном состоянии и названием частицы.
1 — 3s23p6
2 — 4s24p6
3 — 2s22p5
а — атом серы
б — катион калия
в — бромид-ион
г — атом ксенона
д — атом фтора
Одноатомными молекулами (н. у.) образовано простое вещество:
Заряд ядра химического элемента +31. Его относительная атомная масса равна:
Установите соответствие между электронной конфигурацией внешнего энергетического уровня атома (иона) в основном состоянии и названием частицы.
1 — 4s24p5
2 — 3s23p6
3 — 3s23p3
а — катион алюминия
б — атом фосфора
в — хлорид-ион
г — атом брома
д — атом бора
Одноатомными молекулами (н. у.) образовано простое вещество:
Заряд ядра химического элемента +23. Его относительная атомная масса равна:
Установите соответствие между электронной конфигурацией внешнего энергетического уровня атома (иона) в основном состоянии и названием частицы.
1 — 2s22p1
2 — 4s24p3
3 — 5s25p6
а — атом мышьяка
б — иодид-ион
в — катион рубидия
г — атом селена
д — атом бора
Одноатомными молекулами (н. у.) образовано простое вещество:
Заряд ядра химического элемента +20. Его относительная атомная масса равна:
Установите соответствие между электронной конфигурацией внешнего энергетического уровня атома (иона) в основном состоянии и названием частицы.
1 — 5s25p5
2 — 3s23p6
3 — 5s25p3
а — атом сурьмы
б — бромид-ион
в — катион калия
г — атом криптона
д — атом йода
Заряд ядра атома бора равен:
Электронная конфигурация 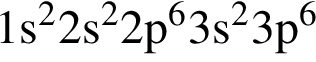 соответствует иону или атому в основном состоянии:
соответствует иону или атому в основном состоянии:
Число протонов в ядре атома ![]() равно:
равно:
Электронная конфигурация атома некоторого элемента в основном состоянии 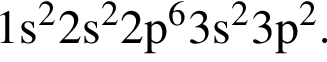 Этому элементу в периодической системе соответствуют группа и номер периода:
Этому элементу в периодической системе соответствуют группа и номер периода:
Число нейтронов в ядре атома ![]() равно:
равно:
Укажите символ химического элемента:
Число нейтронов в составе атома ![]() равно:
равно:
Элемент, атом которого в основном состоянии имеет электронную конфигурацию 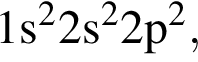 находится в группе:
находится в группе:
Число полностью заполненных энергетических подуровней на внешнем энергетическом уровне атома элемента с порядковым номером 10 в основном состоянии равно:
Согласно положению в периодической системе наиболее выраженные металлические свойства проявляет элемент, электронная конфигурация внешнего энергетического уровня которого в основном состоянии:
Катионом является частица, формула которой:
Число нейтронов в ядре атома ![]()
Заряд ядра атома хлора равен:
Электронная конфигурация 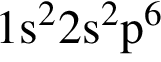 соответствует иону или атому в основном состоянии:
соответствует иону или атому в основном состоянии:
Заряд ядра атома фтора равен:
Электронная конфигурация 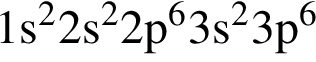 соответствует иону или атому в основном состоянии:
соответствует иону или атому в основном состоянии:
Заряд ядра атома углерода равен:
Электронная конфигурация 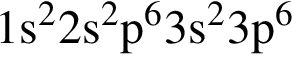 соответствует иону или атому в основном состоянии:
соответствует иону или атому в основном состоянии:
Заряд ядра атома хрома равен:
Электронная конфигурация 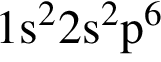 соответствует иону или атому в основном состоянии:
соответствует иону или атому в основном состоянии:
Выберите правильное утверждение:
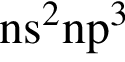
Число нейтронов в ядре атома ![]() равно:
равно:
Число полностью заполненных энергетических подуровней на внешнем энергетическом уровне атома элемента с порядковым номером 7 в основном состоянии равно:
Элемент, имеющий распределение электронов в атоме по энергетическим уровням 2, 8, 4, расположен в периодической системе:
Катионом является частица, формула которой:
Число нейтронов в ядре атома ![]() равно:
равно:
Число завершенных энергетических уровней в основном состоянии атома элемента с порядковым номером 16 равно:
Элемент, имеющий распределение электронов в атоме по энергетическим уровням 2, 8, 3, расположен в периодической системе:
Согласно положению в периодической системе наиболее выраженные металлические свойства проявляет элемент, электронная конфигурация внешнего энергетического уровня которого в основном состоянии:
Число нейтронов в ядре атома ![]() равно:
равно:
Число электронов на внешнем энергетическом уровне сульфид-иона равно:
Число нейтронов в составе атома ![]() равно:
равно:
Элемент, атом которого в основном состоянии имеет электронную конфигурацию 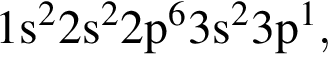 находится в группе:
находится в группе:
Число протонов в ядре атома ![]() равно:
равно:
Электронная конфигурация атома некоторого элемента в основном состоянии 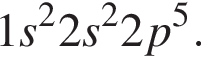 Этому элементу в периодической системе соответствуют группа и номер периода:
Этому элементу в периодической системе соответствуют группа и номер периода:
Число протонов в ядре атома ![]() равно:
равно:
Электронная конфигурация атома некоторого элемента в основном состоянии 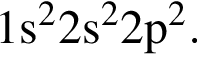 Этому элементу в периодической системе соответствуют группа и номер периода:
Этому элементу в периодической системе соответствуют группа и номер периода:
Число протонов в ядре атома ![]() равно:
равно:
Электронная конфигурация атома некоторого элемента в основном состоянии 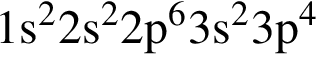 Этому элементу в периодической системе соответствуют группа и номер периода:
Этому элементу в периодической системе соответствуют группа и номер периода:
Число протонов в ядре атома ![]() равно:
равно:
Электронная конфигурация атома некоторого элемента в основном состоянии 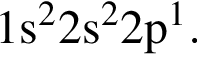 Этому элементу в периодической системе соответствуют группа и номер периода:
Этому элементу в периодической системе соответствуют группа и номер периода:
Укажите символ химического элемента:
Число нейтронов в составе атома ![]() равно:
равно:
Элемент, атом которого в основном состоянии имеет электронную конфигурацию 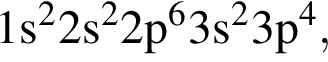 находится в группе:
находится в группе:
Укажите символ химического элемента:
Число нейтронов в составе атома ![]() равно:
равно:
Элемент, атом которого в основном состоянии имеет электронную конфигурацию 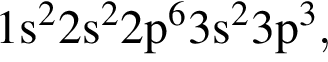 находится в группе:
находится в группе:
Укажите символ химического элемента:
Число нейтронов в составе атома ![]() равно:
равно:
Элемент, атом которого в основном состоянии имеет электронную конфигурацию 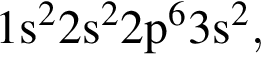 находится в группе:
находится в группе:
В периодической системе в одной группе с аргоном находится химический элемент:
В атоме химического элемента 24 электрона. Его относительная атомная масса равна:
Атом ![]() и анион водорода
и анион водорода ![]() в основном состоянии подобны между собой:
в основном состоянии подобны между собой:
В периодической системе в одной группе с бором находится химический элемент:
В атоме химического элемента 21 электрон. Его относительная атомная масса равна:
Атом ![]() и анион водорода
и анион водорода ![]() в основном состоянии подобны между собой:
в основном состоянии подобны между собой:
В периодической системе в одной группе с кремнием находится химический элемент:
В атоме химического элемента 23 электрона. Его относительная атомная масса равна:
Атом ![]() и анион водорода
и анион водорода ![]() в основном состоянии подобны между собой:
в основном состоянии подобны между собой:
Относительная атомная масса элемента равна 31. Укажите число протонов в ядре атома этого элемента:
Трёхзарядным катионам p-элементов (![]() ) соответствуют электронные конфигурации:
) соответствуют электронные конфигурации:
а) 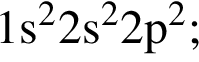
б) 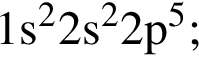
в) 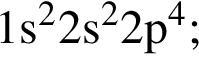
г) ![]()
В атоме некоторого элемента содержится 16 электронов. Укажите символ элемента:
Трёхзарядный катион (Э3+) имеет конфигурацию 1s22s22р5. Укажите число неспаренных электронов в атоме элемента Э в основном состоянии:
Один неспаренный электрон в основном состоянии содержит атом:
Электронная конфигурация атома 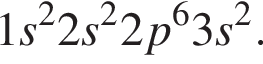 Число энергетических уровней, занятых электронами в атоме, равно:
Число энергетических уровней, занятых электронами в атоме, равно:
Массовое число атома, содержащего 10 нейтронов и 8 электронов, равно:
Электронная конфигурация атома 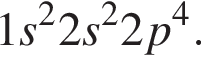 Число энергетических уровней, занятых электронами в атоме, равно:
Число энергетических уровней, занятых электронами в атоме, равно:
Массовое число атома, содержащего 2 нейтрона и 1 электрон, равно:
Атом содержит 37 протонов. Число энергетических уровней, на которых расположены электроны в данном атоме в основном состоянии, равно:
В ряду атомов 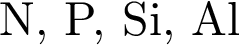 последовательно:
последовательно:
Атом содержит 10 протонов. Число энергетических уровней, на которых расположены электроны в данном атоме в основном состоянии, равно:
Дана электронно-графическая схема атома химического элемента:
Число протонов в ядре атома этого элемента равно:
Дана электронно-графическая схема атома химического элемента:
Число протонов в ядре атома этого элемента равно:
Дана электронно-графическая схема атома химического элемента в основном состоянии:
Его относительная атомная масса равна:
Число протонов в ионе ![]() равно:
равно:
Дана электронно-графическая схема атома химического элемента в основном состоянии:
Его относительная атомная масса равна:
Число протонов в ионе ![]() равно:
равно:
Число нейтронов в нуклиде ![]() равно:
равно:
Электронная конфигурация 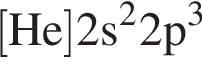 соответствует основному состоянию атома элемента:
соответствует основному состоянию атома элемента:
Число нейтронов в нуклиде ![]() равно:
равно:
Электронная конфигурация  соответствует основному состоянию атома элемента:
соответствует основному состоянию атома элемента:

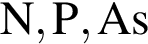 .
.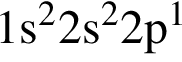 соответствует атому бора, который находится в третьей группе главной подгруппе во втором периоде.
соответствует атому бора, который находится в третьей группе главной подгруппе во втором периоде.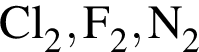 являются молекулами, а не символами. Символы химических элементов представлены в таблице Менделеева.
являются молекулами, а не символами. Символы химических элементов представлены в таблице Менделеева.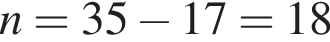
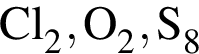 являются молекулами, а не символами. Символы химических элементов представлены в таблице Менделеева.
являются молекулами, а не символами. Символы химических элементов представлены в таблице Менделеева.
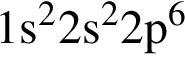
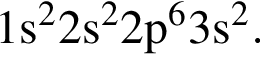 То есть все электроны спарены.
То есть все электроны спарены.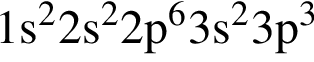 — три неспаренных электрона;
— три неспаренных электрона;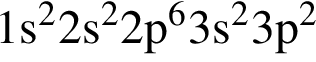 — два неспаренных электрона;
— два неспаренных электрона;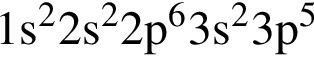 — один неспаренный электрон;
— один неспаренный электрон;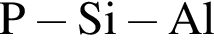 справа налево по группе. Следовательно, в этом ряду элементов последовательно увеличивается радиус атома.
справа налево по группе. Следовательно, в этом ряду элементов последовательно увеличивается радиус атома. нейтронов.
нейтронов.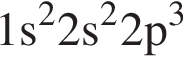 — всего 7 электронов, следовательно, соответствует седьмому элементу в Периодической системе — азоту,
— всего 7 электронов, следовательно, соответствует седьмому элементу в Периодической системе — азоту, 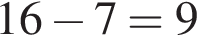 нейтронов.
нейтронов.